Các biến thể di truyền của SARS-CoV-2 — Chúng có ý nghĩa gì?
Article Information
Corresponding Author: Adam S. Lauring, MD, PhD, Division of Infectious Diseases, Department of Internal Medicine and Department of Microbiology and Immunology, University of Michigan, 1150 W Medical Center Dr, MSRB1 5510B, Ann Arbor, MI 48109-5680 ([email protected]).
Published Online: January 6, 2021. doi:10.1001/jama.2020.27124
Trong khi đại dịch hội chứng hô hấp cấp tính do coronavirus 2 (SARS-CoV-2) đang diễn ra rầm rộ khắp nơi trên thế giới mà nguồn gốc còn đang chưa rõ thì cộng đồng y tế công cộng, khoa học và các nhà lâm sàng đã phải ứng phó với các biến thể di truyền vi rút mới. Sự kiện mới này gây ra một loạt sự chú ý của giới truyền thông, hàng loạt phản ứng từ cộng đồng khoa học và lời kêu gọi từ các chính phủ "bình tĩnh" hoặc theo đuổi các biện pháp đối phó ngay lập tức. Trong khi nhiều nhà khoa học ban đầu nghi ngờ về tầm quan trọng của sự thay đổi D614G, thì sự xuất hiện của “biến thể Anh” mới —lineage B.1.1.7 — đã làm dấy lên lo ngại rộng rãi. Hiểu được những biến thể nào đang liên quan đến và tại sao, đòi hỏi phải đánh giá cao sự tiến hóa của virus và dịch tễ học bộ gen của SARS-CoV-2 thì chúng ta mới biết mình cần có thái độ ra sao và làm gì trong thời kì mới này.
Đột biến, biến thể và lây lan
Đột biến phát sinh như một sản phẩm phụ tự nhiên của quá trình nhân lên của virus. Virus RNA thường có tỷ lệ đột biến cao hơn virus DNA. Tuy nhiên, coronavirus tạo ra ít đột biến hơn so với hầu hết các virus RNA vì chúng mã hóa một loại enzyme sửa một số lỗi trong quá trình sao chép. Trong hầu hết các trường hợp, số phận của một đột biến mới phát sinh được quyết định bởi chọn lọc tự nhiên. Những đột biến mang lại lợi thế cạnh tranh liên quan đến sự sao chép, lây truyền hoặc thoát khỏi khả năng miễn dịch của vi rút sẽ tăng tần suất và những đột biến làm giảm khả năng hoạt động của vi rút có xu hướng bị loại bỏ khỏi quần thể vi rút lưu hành. Tuy nhiên, đột biến cũng có thể tăng và giảm tần suất do các sự kiện may rủi. Ví dụ, “hiệu ứng người sáng lập”(founder effect) xảy ra khi một số lượng giới hạn vi rút riêng lẻ thiết lập một quần thể mới trong quá trình lây truyền. Các đột biến hiện diện trong bộ gen của các virut này sẽ thống trị quần thể bất kể ảnh hưởng của chúng đến khả năng sinh sản của virut. Sự tác động lẫn nhau giữa chọn lọc tự nhiên và các sự kiện may rủi này định hình nên sự tiến hóa của virus trong vật chủ, trong cộng đồng và giữa các quốc gia.
Mặc dù các thuật ngữ đột biến, biến thể và chủng thường được sử dụng thay thế cho nhau khi mô tả dịch tễ học của SARS-CoV-2, nhưng sự khác biệt rất quan trọng.
- Đột biến đề cập đến sự thay đổi thực tế trong trình tự: D614G là sự thay thế axit aspartic thành glycine ở vị trí 614 của glycoprotein tăng đột biến.
- Các bộ gen khác nhau về trình tự thường được gọi là các biến thể. Thuật ngữ này hơi kém chính xác hơn vì 2 biến thể có thể khác nhau bởi 1 hoặc nhiều đột biến. Nói một cách chính xác, một biến thể là một chủng khi nó có kiểu hình khác nhau một cách rõ rệt (ví dụ, sự khác biệt về tính kháng nguyên, khả năng truyền nhiễm hoặc độc lực).
Đánh giá một biến thể SARS-CoV-2 mới nên bao gồm đánh giá các câu hỏi sau:
- Biến thể có đạt được sự nổi bật thông qua chọn lọc tự nhiên hoặc các sự kiện ngẫu nhiên không?
- Nếu bằng chứng cho thấy chọn lọc tự nhiên, (những) đột biến nào đang được chọn lọc?
- Lợi ích thích nghi của những đột biến này là gì? Những đột biến này có ảnh hưởng gì đến khả năng truyền và lây lan, tính kháng nguyên hoặc độc lực?
Spike D614G
Đột biến D614G trong glycoprotein tăng đột biến của SARS-CoV-2 lần đầu tiên được phát hiện ở mức đáng kể vào đầu tháng 3 năm 2020 và lan rộng ra toàn cầu trong tháng tiếp theo. Đột biến ban đầu xuất hiện độc lập và đồng thời xảy ra nhiều lãnh thổ. Sự tiến hóa này gợi ý đến sự chọn lọc tự nhiên và một lợi ích thích nghi của D614G. Tuy nhiên, những nỗ lực giải trình tự tiếp theo đã xác định được đột biến D614G trong virus ở một số tỉnh của Trung Quốc vào cuối tháng Giêng. Điều này làm tăng khả năng phát tán toàn cầu của đột biến, trong đó vi rút chứa 614G chỉ tình cờ bắt đầu phần lớn các sự kiện lây truyền sớm ở nhiều địa điểm.
Giả thuyết vô hiệu hợp lý này khiến nhiều người trong cộng đồng tiến hóa nghi ngờ rằng đột biến D614G có khả năng thích nghi, mặc dù dữ liệu in vitro cho thấy tăng tác động của nó đối với liên kết thụ thể. Một phân tích di truyền và phân tích động lực học quần thể gần đây của hơn 25 000 trình tự từ Vương quốc Anh cho thấy rằng vi rút mang 614G dường như lây lan nhanh hơn và tạo ra các cụm phát sinh loài lớn hơn so với vi rút mang 614D. Gần đây, nghiên cứu bổ sung trên các mô hình động vật chỉ ra rằng vi rút 614G lây truyền mạnh hơn.
Spike N453Y và Mink
Liên quan đến sự bùng phát của SARS-CoV-2 bắt đầu nổi lên ở các trang trại nuôi chồn hương ở Hà Lan và Đan Mạch vào cuối mùa xuân và đầu mùa hè năm 2020. Điều tra gen và dịch tễ học về một đợt bùng phát sớm ở Hà Lan đã chứng minh người với chồn, chồn với chồn và chồn sang người. Vào đầu tháng 11 năm 2020, các nhà chức trách Đan Mạch đã báo cáo 214 trường hợp mắc bệnh do coronavirus ở người 2019 (COVID-19) liên quan đến các trang trại nuôi chồn hương. Nhiều trình tự SARS-CoV-2 từ các đợt bùng phát ở Hà Lan và Đan Mạch có đột biến Y453F trong vùng liên kết thụ thể tăng đột biến, có thể làm tăng ái lực liên kết với thụ thể ACE2 (enzym chuyển angiotensin 2). Mười một cá thể từ đợt bùng phát ở Đan Mạch có một biến thể được gọi là cụm 5, có thêm 3 đột biến tăng đột biến (del69_70, I692V và M1229I). Một cuộc điều tra ban đầu trên 9 mẫu huyết thanh dưỡng bệnh ở người cho thấy mức độ giảm hoạt động trung hòa có ý nghĩa thống kê ở mức độ khác nhau đối với virus nhóm 5 (trung bình 3,58 lần; CI, 0-13,5). Tuy nhiên, sự thích nghi rõ ràng của SARS-CoV-2 với chồn là điều đáng lo ngại vì sự tiến hóa liên tục của vi rút trong ổ chứa động vật có khả năng dẫn đến các sự kiện lan truyền lặp lại của SARS-CoV-2 mới từ chồn sang người và các động vật có vú khác. Vì lý do này, nhiều quốc gia đã tăng cường nỗ lực giám sát và trong một số trường hợp đã thực hiện tiêu hủy quy mô lớn (tức là giết mổ chọn lọc) chồn tại các trang trại.
Lineage B.1.1.7 và N501Y
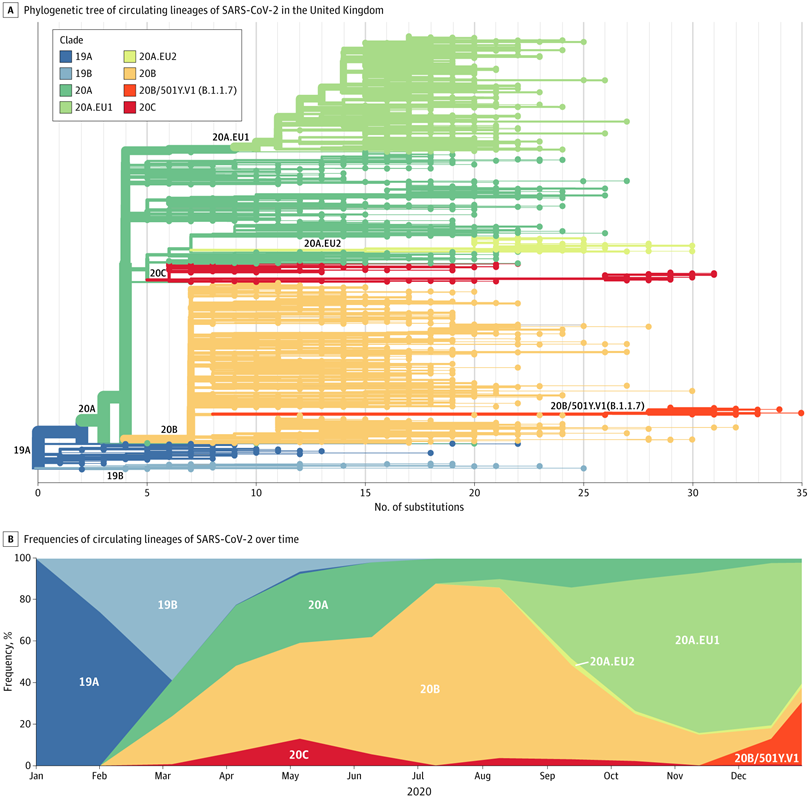
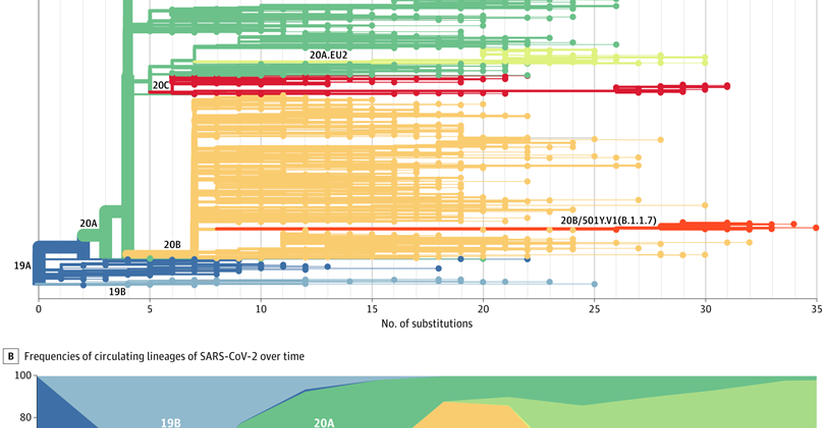
Lineage B.1.1.7 (còn được gọi là 501Y.V1) là một cụm phát sinh loài đang lan rộng nhanh chóng ở đông nam nước Anh ( Hình ). Nó đã tích lũy 17 đột biến xác định dòng dõi trước khi được phát hiện vào đầu tháng 9, điều này cho thấy một lượng đáng kể quá trình tiến hóa trước đó, có thể ở một vật chủ bị nhiễm bệnh mãn tính. Tính đến ngày 28 tháng 12 năm 2020, biến thể này chiếm khoảng 28% các trường hợp nhiễm SARS-CoV-2 ở Anh, và các mô hình di truyền quần thể cho thấy nó lây lan nhanh hơn 56% so với các dòng khác. Không giống như D614G, dòng B.1.1.7 dường như đã đạt được ưu thế bằng cách vượt qua một quần thể hiện có của các biến thể đang lưu hành để trở thành quần thể lan rộng hơn. Điều này gợi ý rõ ràng về sự chọn lọc tự nhiên đối với một loại virus dễ lây truyền hơn ở cấp độ quần thể. Trong khi các biện pháp can thiệp sức khỏe cộng đồng như khẩu trang, cách xa thể chất và các hạn chế đối với các cuộc tụ tập đông người vẫn có hiệu quả, việc kiểm soát một biến thể dễ lây truyền hơn có thể sẽ đòi hỏi áp dụng nghiêm ngặt hơn và áp dụng rộng rãi các biện pháp này.
Tám trong số các đột biến dòng B.1.1.7 nằm trong glycoprotein tăng đột biến, bao gồm N501Y trong vùng liên kết thụ thể, xóa 69_70, và P681H ở vị trí phân cắt furin. Tất cả những đột biến này có thể ảnh hưởng một cách hợp lý đến sự gắn kết ACE2 và sự nhân lên của virus. Các biến thể đột biến 501Y được dự đoán có ái lực cao hơn với ACE2 ở người và một biến thể khác, cũng mang đột biến N501Y, đang nhanh chóng lây lan ở Nam Phi. Ảnh hưởng của những đột biến này đối với tính kháng nguyên hiện chưa rõ ràng.
Tính kháng nguyên và hiệu quả của vắc xin
Giám sát bộ gen của các biến thể SARS-CoV-2 chủ yếu tập trung vào các đột biến trong glycoprotein tăng đột biến, làm trung gian gắn vào tế bào và là mục tiêu chính của các kháng thể trung hòa. Người ta quan tâm nhiều đến việc liệu các đột biến trong trung gian glycoprotein tăng đột biến có thoát khỏi các kháng thể vật chủ và có thể ảnh hưởng đến hiệu quả của vắc xin hay không, vì đột biến là kháng nguyên vi rút chính trong các vắc xin hiện tại. Tại thời điểm này, việc lựa chọn mạnh mẽ một biến thể ở cấp độ quần thể có lẽ không phải do kháng thể vật chủ thúc đẩy vì không có đủ số lượng cá thể miễn dịch để đẩy vi rút một cách có hệ thống theo một hướng nhất định. Ngược lại, nếu một biến thể có một hoặc nhiều đột biến tăng đột biến làm tăng khả năng lây truyền, nó có thể nhanh chóng cạnh tranh và thay thế các biến thể đang lưu hành khác.
Tách nguyên nhân khỏi hậu quả là điều quan trọng trong việc đánh giá dữ liệu về sự trung hòa kháng thể của các biến thể đột biến. Bất kể lý do tại sao các đột biến được lựa chọn, điều hợp lý để mong đợi rằng nhiều đột biến tăng đột biến có thể ảnh hưởng đến quá trình trung hòa bằng huyết thanh dưỡng bệnh. Do đó, điều quan trọng là phải xem xét cả mức độ thay đổi độ trung hòa và số lượng mẫu huyết thanh được đánh giá. Một vấn đề khác là các glycoprotein của virus phải đánh đổi quá trình tiến hóa. Đôi khi một đột biến làm tăng cường một đặc tính của virus, chẳng hạn như liên kết với một thụ thể, có thể làm giảm một đặc tính khác, chẳng hạn như thoát khỏi kháng thể của vật chủ. Thật vậy, bằng chứng gần đây cho thấy đây có thể là trường hợp của D614G. Có thể là các đột biến tăng đột biến “tốt” cho vi rút ngay bây giờ cũng có thể làm cho nó kém phù hợp hơn trong bối cảnh miễn dịch ở cấp độ quần thể trong tương lai. Việc xác định các động lực này và ảnh hưởng tiềm tàng của chúng đến hiệu quả của vắc xin, sẽ đòi hỏi phải theo dõi quy mô lớn về sự tiến hóa của SARS-CoV-2 và khả năng miễn dịch của vật chủ trong một thời gian dài sắp tới.
References
1.Grubaugh ND, Petrone ME, Holmes EC. We shouldn’t worry when a virus mutates during disease outbreaks. Nat Microbiol. 2020;5(4):529-530. doi:10.1038/s41564-020-0690-4PubMedGoogle ScholarCrossref
2. Korber B, Fischer WM, Gnanakaran S, et al; Sheffield COVID-19 Genomics Group. Tracking changes in SARS-CoV-2 spike: evidence that D614G increases infectivity of the COVID-19 virus. Cell. 2020;182(4):812-827.e19. doi:10.1016/j.cell.2020.06.043PubMedGoogle ScholarCrossref
3. Volz E, Hill V, McCrone JT, et al; COG-UK Consortium. Evaluating the effects of SARS-CoV-2 spike mutation D614G on transmissibility and pathogenicity. Cell. 2020;S0092867420315373.PubMedGoogle Scholar
4. Plante JA, Liu Y, Liu J, et al. Spike mutation D614G alters SARS-CoV-2 fitness. Nature. Published online December 23, 2020. doi:10.1038/s41586-020-2895-3Google Scholar
5. Hou YJ, Chiba S, Halfmann P, et al. SARS-CoV-2 D614G variant exhibits efficient replication ex vivo and transmission in vivo. Science. 2020;370(6523):1464-1468. doi:10.1126/science.abe8499PubMedGoogle Scholar
6. European Centre for Disease Prevention and Control. Detection of new SARS-CoV-2 variants related to mink. Posted November 12, 2020. Accessed January 3, 2021. https://www.ecdc.europa.eu/.../RRA-SARS-CoV-2-in-mink-12...
7. Oude Munnink BB, Sikkema RS, Nieuwenhuijse DF, et al. Transmission of SARS-CoV-2 on mink farms between humans and mink and back to humans. Science. 2020;eabe5901. doi:10.1126/science.abe5901PubMedGoogle Scholar
8. Rambaut A, Loman N, Pybus O, et al; COVID-19 Genomics Consortium UK. Preliminary genomic characterisation of an emergent SARS-CoV-2 lineage in the UK defined by a novel set of spike mutations. Virological.org. Posted December 16, 2020. Accessed January 3, 2021. https://virological.org/.../preliminary-genomic.../563
9. Davies NG, Barnard RC, Jarvis CI, et al Estimated transmissibility and severity of novel SARS-CoV-2 Variant of Concern 202012/01 in England. CMMID. Preprint published online December 23, 2020. Updated December 31, 2020. doi:10.1101/2020.12.24.20248822
10. Weissman D, Alameh M-G, de Silva T, et al. D614G spike mutation increases SARS CoV-2 susceptibility to neutralization. Cell Host Microbe. 2020;S193131282030634X.PubMedGoogle Scholar
- Tags:
- infectious disease
- nCoV
- corona
- COVID-19

0 Bình luận:
Gửi trả lời
Please login to comment